Респираторная медицина. Руководство (в 2-х томах) - Чучалин А. Г. (читать хорошую книгу .txt) 📗
path: pictures/0457.png
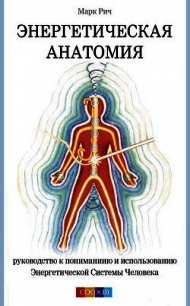
Рис. 4-57. Взаимоотношение путей рециркуляции лимфоцитов.
Лимфоцитам слизистой оболочки бронхов свойственен и другой путь миграции - базоапикальный, т.е. перемещение из глубины слизистой оболочки в просвет бронха. Это направленное движение в случае Тклеток определяется взаимодействием молекулы LFA1 их поверхности с молекулой ICAM1 окружающих клеток. Важную роль в миграции играют также бета1интегрин VLA4 и компоненты межклеточного матрикса, служащие его рецепторами. Направление движения определяется градиентом хемокина CCL5 (RANTES) [29].
ФУНКЦИОНИРОВАНИЕ ОТДЕЛА ИММУННОЙ СИСТЕМЫ, СВЯЗАННОГО С СИСТЕМОЙ ДЫХАНИЯ
Функционирование иммунной системы в воздухопроводящих путях и легких существенно различается в зависимости от наличия или отсутствия антигенного воздействия, а также от его природы и повторности.
Функционирование в условиях стерильности. Эта ситуация практически не реализуется в действительности и соответствует идеальной ситуации полного отсутствия антигенной нагрузки. Индуктивная составляющая НАЛТ находится в процессе формирования. БАЛТ отсутствует. В слизистой оболочке содержится минимальное число наивных лимфоцитов, но присутствуют дендритные клетки, макрофаги и другие разновидности клеток врожденного иммунитета. Lamina propria бронхов и интерстиция легких заселены клетками, мигрирующими из крови. Функционирование аппарата состоит в медленной миграции лейкоцитов (в том числе лимфоцитов) из крови в подслизистый слой воздухоносных путей и интерстициальную ткань легких, а также в слабой, но непрерывной миграции дендритных клеток из слизистой оболочки в региональные лимфатические узлы: из верхних дыхательных путей - в шейные и подъязычные, из нижних дыхательных путей - в медиастинальные. Мигрирующие дендритные клетки не активированы. Они содержат в составе молекул МНС фрагменты аутологичных макромолекул. Этот процесс необходим для формирования Тзависимых зон вторичных лимфоидных органов и обеспечения выживаемости Тлимфоцитов.
Функционирование в условиях поступления аэроантигенов, не связанных с патогенами. Последствия поступления в организм вдыхаемых антигенов весьма существенно зависят от того, содержат ли они ПАМП - молекулярные паттерны («образы»), связанные с патогенами (см. выше), например бактериальные липополисахариды, гликолипиды, пептидогликаны, нуклеиновые кислоты патогенов и другие субстанции, распознаваемые TLрецепторами клеток иммунной системы. Если таковые отсутствуют во вдыхаемом антигенном материале, не происходит активации макрофагов, дендритных, эпителиальных и других клеток через TLрецепторы, не происходит выделения провоспалительных цитокинов и последующего развития не только воспалительной реакции, но и иммунного ответа.
В этом случае антиген доставляется во внутреннюю среду организма путем активного транспорта Мклетками или с помощью захвата отростками внутриэпителиальных дендритных клеток; реже происходит его пассивное всасывание. В случае транспорта через Мклетку антиген захватывается дендритными клетками или достигает региональных лимфоузлов с лимфой. В связи с отсутствием активации макрофагов, эпителиальных и самих дендритных клеток среди гуморальных продуктов, секретируемых названными клетками, отсутствуют провоспалительные цитокины. В то же время в межтканевой среде содержатся супрессорные факторы - TGFбета, спонтанно выделяемый эпителиальными клетками, IL10, секретируемый дендритными клетками, и простагландин PGE2, который вырабатывается макрофагами. Все перечисленные продукты предотвращают активацию дендритных клеток и индуцируют «толерогенный» фенотип дендритных клеток [30]. Эти клетки в обычном ритме поступают в лимфу и доставляются в региональные лимфатические узлы. В процессе миграции не происходит усиления экспрессии костимулирующих молекул CD80, CD86 и других и не индуцируется синтез IL12. В результате при контакте таких толерогенных дендритных клеток с CD4<sup>+</sup> Тклетками в тимусзависимых зонах лимфоузлов не происходит активации Тклеток, их последующей пролиферации и дифференцировки в Тхелперы. Напротив, индуцируется анергия Тклеток, часто завершающаяся их ускоренной гибелью. Может происходить также развитие регуляторных Тклеток (Treg). Результатом этих процессов является индукция иммунологической толерантности (неотвечаемости) к аэрогенным антигенам [31]. Так аэрогенное введение растворимого белка овальбумина вызывает развитие толерантности к этому антигену. Этот механизм чрезвычайно важен для поддержания толерантности к собственным антигенам организма. Его нарушение вызывает аутоиммунную патологию.
Функционирование иммунологических структур органов дыхания в условиях первичного поступления аэроантигенов, связанных с патогенами. В тех случаях, когда через воздухоносные пути поступают патогены или их ПАМПсодержащие продукты, распознаваемые TLрецепторами, включается цепь событий, индуцирующих иммунный ответ (рис. 4-58).
path: pictures/0458.png
Рис. 4-58. Схема развития иммунного ответа в легких.
Вирусные и бактериальные антигены обычно проникают вначале через слизистую оболочку носоглотки. Значительная часть чужеродного материала удаляется механически на уровне верхних дыхательных путей. Бронхов достигают лишь наиболее мелкие корпускулярные частицы. Как и в предыдущем случае, антигенный материал транспортируется в ткань НАЛТ Мклетками или, минуя НАЛТ, захватывается межэпителиальными отростками дендритных клеток. Возможно также активное проникновение патогенов через слизистую оболочку благодаря участию ферментов микроорганизмов, содержащихся в просвете дыхательных путей. В случае наличия БАЛТ аналогичные процессы могут происходить и в нижних дыхательных путях, хотя антигенная нагрузка на них заведомо ниже.
Поступление в организм патогенов и их продуктов сопряжено с активацией эпителиальных клеток, макрофагов, тучных и дендритных клеток, вследствие распо-знавания молекулярных структур (паттернов), связанных с патогенами, TLрецепторами. Макрофаги и эпителиальные клетки продуцируют провоспалительные цитокины (IL1, TNFальфа, хемокины и т.д.), участвующие в запуске воспалительной реакции.
В случае поступления антигена с участием НАЛТ/БАЛТзависимого пути он оказывается в субэпителиальном кармане, под которым локализуются дендритные клетки (см. рис. 4-56). При первичном иммунном ответе на этом этапе, повидимому, не происходит диалога дендритных клеток с наивными лимфоцитами. Дендритные клетки, захватившие антиген, активируются - как непосредственно лигандами TLрецепторов, так и цитокинами, вырабатываемыми макрофагами, особенно TNFальфа. Это ускоряет поступление дендритных клеток в афферентную лимфу лимфатических узлов.
В процессе миграции происходит переработка антигена и его включение в состав молекул МНС классов I и II, причем экспрессия последних, а также костимулирующих молекул CD80 и CD86 усиливается. Дендритные клетки в ответ на сигнал хемокинов CCL19 и CCL2 проникают в тимусзависимую область (паракортикальную зону) регионального лимфоузла. Здесь они секретируют IL12 и упомянутые хемокины, которые привлекают к ним Тклетки. При контакте дендритных клеток и Тлимфоцитов происходит распознавание Тклетками, несущими соответствующий рецептор, комплексов МНСпептид, экспрессируемых дендритными клетками. В результате происходит активация Тклеток данного клона.
Во взаимодействие с дендритными клетками и последующую активацию вовлекаются как CD4<sup>+</sup>, так и CD8<sup>+</sup> Тклетки. Первые дифференцируются в Тхелперы, преимущественно Th1типа, которые секретируют IFNгамма, IL2 и ряд других цитокинов, необходимых для развития иммунного ответа воспалительного типа. Его эффекторами служат макрофаги, активируемые IFNгамма. Активация макрофагов, фагоцитировавших патогены, приводит к активации бактерицидных механизмов, что способствует элиминации внутриклеточных патогенов, локализующихся в эндосомах (например, микобактерий). Одновременно образуются также Th2хелперы, которые секретируют IL4, IL5 и другие цитокины, участвующие в развитии гуморального иммунного ответа, а также в осущеcтвлении антипаразитарной защиты. CD8<sup>+</sup> клетки под влиянием активации антигеном, презентируемым дендритными клетками, дифференцируются в цитотоксические Тлимфоциты, которые реализуют защиту от внутриклеточных патогенов (вирусов, простейших), белки которых присутствуют в цитоплазме. Именно цитотоксические CD8<sup>+</sup> Тлимфоциты являются основными эффекторными клетками, которые определяют защиту от вирусов гриппа, респираторного синцитиального вируса.